Jorge Rodríguez B.(1), Jane C. Wheeler(1,2), Ciara S. Dodd(3), Michael W. Bruford(3) y
Raúl Rosadio A.(1,4)
Abstract
Ten polymorphic microsatellites for alpacas and llamas were used to evaluate paternity
in 47 alpacas (18 crias, 18 mothers and 11 fathers) registered at IVITA-Maranganí Research
Station, Canchis Province (Cusco-Peru). Analysis was carried out using two
methodologies: Automatic Sequencer (ABI 377 DNA sequencers®) and silver staining
techniques. Microsatellites were amplified in three multiple and ten single PCR reactions.
The number of alleles varied between 4 and 20. The allelic frequencies and the exclusion
probability were calculated using Cervus 2.0. All loci, except for two, were within the
range published elsewhere. The accumulated exclusion probability for the ten loci was
0.9999. For each multiplex reaction the accumulated exclusion probability was more than
0.90. Both methodologies yielded the same results. The results confirmed paternity in 18
cases of parent-cria pairs, however in 22% of cases (n=4) were identified alternative
parents than those indicated in farm records.
Key words: alpaca, microsatellites, paternity
Resumen
Diez microsatélites polimórficos para alpacas y llamas fueron usados para evaluar el
parentesco en 47 alpacas (18 crías, 18 madres y 11 padres) de la Estación Experimental
IVITA-Maranganí, provincia de Canchis (Cusco, Perú). El análisis se llevó a cabo utilizando
dos metodologías: secuenciador automático (ABI 377 DNA sequencers®) y técnica
de tinción con nitrato de plata. Los microsatélites fueron amplificados en tres reacciones
de PCR múltiple y diez reacciones de PCR simple. El número de alelos varió entre 4 y
20. Las frecuencias alélicas y la probabilidad de exclusión (PE) fueron calculadas utilizando
el software Cervus 2.0. Todos los loci, a excepción de dos, se encontraron dentro de
los rangos encontrados en la literatura. La probabilidad de exclusión acumulada para los
10 loci fue 0.9999. La probabilidad de exclusión acumulada para cada reacción de PCR
múltiple fue mayor a 0.90. Ambas metodologías obtuvieron los mismos resultados. Los
resultados confirmaron la paternidad en 18 casos; sin embargo en el 22% de los casos
(n=4) se identificaron padres alternativos que no correspondieron a los padres registrados.
Palabras clave: alpaca, microsatélites, paternidad
Introducción
Métodos precisos para identificación y
verificación de parentesco son de gran importancia
para los criadores de animales domésticos,
así como para el establecimiento
de registros y libros genealógicos. Por muchos
años, los métodos convencionales, tales
como la tipificación de grupos sanguíneos y
polimorfismos bioquímicos han sido las únicas
herramientas utilizadas para dicho fin.
Durante la pasada década se han desarrollado
técnicas basadas en ADN y puestas en
práctica mediante la técnica de la reacción
en cadena de la polimerasa (PCR).
Entre
estas técnicas se encuentra el análisis de
ADN microsatélite.
Los microsatélites, comúnmente conocidos
como repeticiones cortas en serie
(STRs), son secuencias cortas (no mayores
de 6 pares de bases de largo) repetidas en
serie (Hancock, 1991) que pueden ser amplificados
por la técnica de PCR y los distintos
alelos observados por medio de electroforesis
en gel y posterior teñido con nitrato de plata
o por marcado con sustancias fluorescentes.
En países como EE.UU, Canadá, Reino
Unido y Australia, el ingreso de camélidos
a libros de registro se basa en el análisis de
ADN (microsatélites) para identificación individual
y de parentesco.
En el Perú, a diferencia
de estos países, se cuenta con un libro
de registro que acredita la descendencia de
los animales inscritos, por medio de técnicas
que tienen un grado de certeza muy inferior
a las obtenidas por pruebas genéticas aceptadas
en países con mayor desarrollo tecnológico.
Por lo tanto, se vuelve necesario contar
con una prueba de análisis de ADN de
alta confiabilidad, de costo moderado y que
pueda ser aplicado en forma masiva con la
tecnología disponible en el país.
Materiales y Métodos
Se colectó sangre de 47 alpacas
(Vicugna pacos) previamente identificadas
(11 padres, 18 madres y 18 crías) en los registros
de la Estación Experimental del
IVITA-Maranganí, para la prueba de determinación
de parentesco. El Centro Experimental
se encuentra en el distrito de Maranganí,
provincia de Canchis, departamento de
Cusco, y los análisis se realizaron en las instalaciones
de la Unidad de Virología y Genética
Molecular de la Facultad de Medicina
Veterinaria de la Universidad Nacional Mayor
de San Marcos, Lima, y en la Unidad de
Biodiversidad y Procesos Ecológicos de la
Universidad de Cardiff, Gales, Reino Unido.
El ADN genómico fue extraído de la
sangre utilizando el ULTRACLEAN DNA
BloodSpin Kit® (Mo Bio Inc) de acuerdo a
las instrucciones del fabricante.
La calidad
(tamaño del fragmento) y la cantidad (concentración)
del ADN fue determinada comparando
diluciones seriadas de un marcador
de peso molecular (DNA Hind III®,
AMRESCO a una concentración de 50 ng/µl
en un gel de agarosa al 0.8%.
Los diez loci microsatélite (LCA19,
LCA22, LCA5, LCA23, YWLL08, YWLL29, YWLL36, YWLL40, YWLL43,
YWLL46) designados para llama (Lama
glama) y alpaca, descritos por Lang et al.
(1996) y Penedo et al. (1998) fueron amplificados
por medio de la técnica de reacción en
cadena de la polimerasa (PCR) en un
termociclador modelo 9700 GeneAmp®
(Perkin Elmer) mediante dos métodos. El primero
consistió en tres reacciones de PCR
múltiple (amplificación de más de un locus
por reacción de PCR) y su análisis mediante
un sistema automatizado (ABI 377 DNA
sequencers®); y el segundo consistió en diez
reacciones de PCR de locus simple (amplificación
de un solo locus por reacción de PCR)
y su análisis mediante un sistema no automatizado
de tinción con nitrato de plata (Bassam
et al., 1991).
La asignación de paternidad fue dada
por exclusión, observando incompatibilidades
entre los tamaños de alelos del padre, de la
madre y de las crías, para lo cual se estableció el poder de la prueba de parentesco por
medio de la probabilidad de exclusión individual
y acumulada descritas por Jamieson y
Taylor (1997). Para el análisis de la probabilidad
de exclusión individual y acumulada, la
heterocigocidad observada y el contenido de
información polimórfica (PIC) se utilizó el
software Cervus 2.0 Parentage Analysis ©.
Resultados y Discusión
La determinación de parentesco o paternidad
por medio del análisis de microsatélites
está difundido en muchas de las especies
domésticas y es utilizada con frecuencia
en animales silvestres. Los elevados índices
de confiabilidad permiten el uso de
microsatélites en estudios de paternidad en
caninos con 92% de certeza (Morera et al.,
1999; Pádár et al., 2001), bóvidos domésticos
y silvestres con porcentajes cercanos al
100% (Kankan y Fado, 1999; Mommens et
al., 1998), equinos con niveles cercanos al
100% (Binns et al., 2000) y en primates no
humanos con 99% de certeza (Constable et
al., 2001; Vigilant et al., 2001).
Similares aplicaciones
se observan en camélidos, donde
Sasse et al. (2000) y Sam et al. (2001) demostraron
la factibilidad de realizar pruebas
de paternidad en camellos (Camelus
dromedarius) y Skidmore et al. (1999) en
paternidad de híbridos de camello y guanaco.
La disponibilidad de información sobre
ADN microsatélite en camélidos sudamericanos
permitió diseñar el presente estudio,
en el cual se eligieron diez microsatélites específicos
y altamente polimórficos para
camélidos sudamericanos. En el estudio se
encontró que los diez microsatélites analizados
amplificaron y presentaron polimorfismo
en alpacas, con un número de alelos que varió
entre cuatro para el locus LCA22,
YWLL46 y 20 para el locus YWLL08, con
un promedio de 9.1 alelos por locus; resultados
similares a los publicados por Lang et al.
(1996) y Penedo et al. (1998) aunque con
ligeras variaciones en el YWLL08 y el
YWLL36, posiblemente debido al distinto origen
de los animales.
La probabilidad de exclusión hallada
para cada loci microsatélite varió entre 0.174
para el YWLL46 y 0.844 para el YWLL08,
mostrando diferencias considerables en los
microsatélites YWLL29, YWLL40,
YWLL46, YWLL08 y YWLL36 (diferencia
mayor o menor al 0.1) con respecto a lo publicado
por Lang et al. (1996) y Penedo et
al. (1998). La probabilidad de exclusión acumulada
para los 10 microsatélites fue 0.9999.
Las tres reacciones PCR múltiple obtuvieron
una elevada probabilidad de exclusión combinada
(>0.90). Además, se identificaron cuatro
microsatélites altamente informativos basados
en su alta probabilidad de exclusión individual
(YWLL08, YWLL36, LCA23 y
YWLL29). La probabilidad de exclusión individual
y acumulada para los diez loci
microsatélite así como para las tres PCRs
múltiples se muestran en el Cuadro 1.
Los análisis de exclusión de paternidad
determinaron cuatro errores (22%) en la asignación
de paternidad de los 18 casos evaluados
en base a los registros de la Estación
Experimental IVITA-Maranganí.
Se encontró,
además, un caso en el cual no se pudo
determinar el verdadero padre debido a su
ausencia en las muestras colectadas, lo cual
demuestra la importancia del uso de pruebas
moleculares en la determinación de parentesco.
Una limitante para el análisis de
microsatélites en el país, es la dificultad de
uso de equipos de análisis automatizados en
forma rutinaria, los que se encuentran limitados
a pocas instituciones de investigación
debido a su elevado costo.
En el estudio se
utilizaron dos metodologías: un análisis automatizado
(secuenciador automático) y un
análisis convencional (tinción con nitrato de
plata) obteniéndose los mismos resultados, lo
cual hace posible utilizar un sistema de análisis
convencional en estudios de determinación
de paternidad (Figs. 1 y 2). Se debe precisar
que la técnica de tinción con nitrato de plata
tiene como limitante que analiza un sólo
microsatélite por reacción de PCR, alargando
el tiempo del análisis; sin embargo, se observó la factibilidad del uso de PCR múltiple
(más de un microsatélite) en geles teñidos
con nitrato de plata, para microsatélites con
grandes diferencias de tamaño de sus
alelos, permitiendo disminuir el tiempo y
los costos de la prueba.
Éste es el primer estudio a nivel
molecular diseñado en el país para pruebas
de parentesco en camélidos sudamericanos,
siendo posible su aplicación en llamas
y camélidos silvestres con los marcadores
microsatélites utilizados.
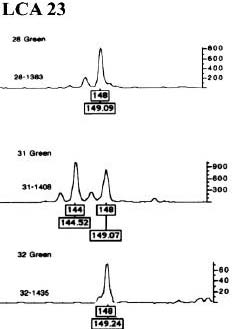 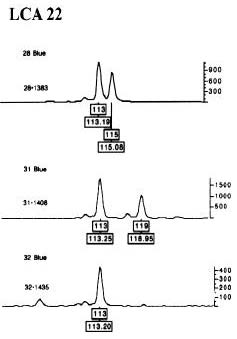
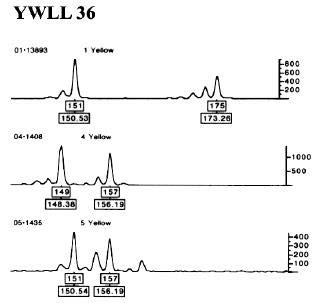
Figura 1. Lectura de los loci LCA23, LCA22 y YWLL36 de alpacas utilizando el software GeneScan 2.1
y Genotyper 2.5 (ABI PRISM)
(a) Lectura del locus LCA23 marcado con el colorante TET (verde). Los números 28, 31 y 32
corresponden a las muestras 1383 (Padre), 1408 (Madre) y 1435 (Cría). Nótese que la
cría (homocigoto para el alelo 148) comparte un alelo con el padre (148) y otro con la
madre (148).
(b) Lectura del locus LCA22 marcado con colorante FAM (azul).
(c) Lectura del locus YWLL36 marcado con el colorante HEX (amarillo). A la derecha se
observa el rango de intensidad de fluorescencia.
Cuadro 1. Heterocigocidad observada (H(o)), contenido de información polimórfica (PIC) y
probabilidad de exclusión individual (PE) y acumulada (PEa) de microsatélites
utilizados para determinar parentesco y paternidad en alpacas
 |
PCR Múltiple |
Microsatélites |
H(o) |
PIC |
PE |
PEa |
|
M1 |
LCA 19 |
0.702 |
0.709 |
0.548 |
0.9191 |
YWLL 29 |
0.787 |
0.786 |
0.634 |
|
YWLL 40 |
0.660 |
0.604 |
0.408 |
|
YWLL 46 |
0.383 |
0.307 |
0.174 |
|
| |
|
|
|
|
|
|
|
|
|
|
|
M2 |
LCA 23 |
0.638 |
0.779 |
0.621 |
0.9286 |
LCA 22 |
0.511 |
0.477 |
0.294 |
|
YWLL 36 |
0.894 |
0.852 |
0.733 |
|
| |
|
|
|
|
|
|
|
|
|
|
|
M3 |
YWLL 43 |
0.304 |
0.639 |
0.452 |
0.9637 |
LCA 5 |
0.809 |
0.744 |
0.575 |
|
YWLL 08 |
0.915 |
0.918 |
0.844 |
|
|
M1+M2+M3 |
10 Microsatélites |
|
|
|
0.9998 |
 |
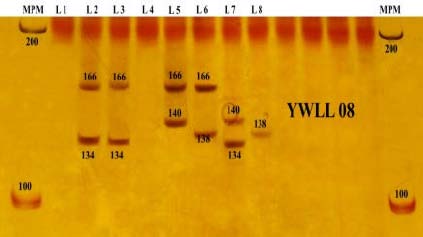
Figura 2. Lectura del locus YWLL 08 de alpacas para la determinación de parentesco utilizando la
técnica de tinción con nitrato de plata (Uso de PCR simple).
Lectura del locus YWLL 08 para la obtención de patrones alélicos. MPM = Marcador de
Peso Molecular (Eco1471/PvuI) L1 = Blanco, L2 = Patrón alelos 134 y 166, L3 = Alegado
Padre 2, L4 = Blanco, L5 = Cría, L6= Madre, L7 = Verdadero Padre y L8 = Patrón alelo 138.
Conclusiones
Se demostró la factibilidad del uso de
ADN microsatélite (diez microsatélites)
para la determinación de parentesco
con una elevada probabilidad
de exclusión (0.9999).
Con el uso de sólo tres microsatélites
(YWLL43, LCA5 y YWLL08) en una
reacción de PCR múltiple es posible
determinar parentesco con una probabilidad
de exclusión aceptable
(0.9637).
Es posible extrapolar los resultados
obtenidos mediante el uso de un equipo
de secuenciamiento automático
(ABI 377 DNA sequencers® Applied
Biosystems) con la metodología de
tinción de plata, con la diferencia del
uso de un solo locus por reacción de
PCR.
Agradecimiento
Los autores agradecen a la Iniciativa
Darwin del Gobierno Británico y
CONOPA (Perú) por el financiamiento y
soporte tecnológico utilizado en este trabajo
de investigación; al Ing. Zootec. Juan
Olazábal (IVITA-Maranganí) por el apoyo
en la toma de muestras, a la MV Rosa
Dávalos (IVITA-Huancayo) y a la MV
Matilde Fernández por estudios preliminares
al presente trabajo. Así mismo, a las
autoridades y personal del IVITA-Maranganí
por permitir la colección de muestras y apoyo
logístico.
Literatura Citada
1. Bassam, B.J.; G. Caetano-Anolles; P.M.
Gresshoff. 1991. Fast and sensitive silver
staining of DNA in polyacrilamide gels. Ann.
Biochem. 19: 680-683.
2. Binns, M.; J. Swinburne; M. Breen.
2000. Molecular genetics of the horse. En:
The genetics of the horse. p 109-121 A.
Bowling; A. Ruvinsky (eds). CABI
Publishing. London.
3. Constable, J.; M. Ashley; J. Goodall; A.
Pusey. 2001. Noninvasive paternity
assignment in Gombe chimpazees.
Molecular Ecology 10: 1279-1300.
4. Hancock, J. 1991. Microsatellites and
other simple sequences: genomic context
and mutational mechanisms. En:
Microsatellites. Evolution and applications.
p 1-9. Goldstein D; C. Schlötterer (eds).
Oxford University Press. Oxford.
5. Jamieson, A.; C.S. Taylor. 1997.
Comparisons of three probability formulae
for parentage exclusion. Animal Genetics
28: 397-400.
6. Kankan, D.; M. Fado. 1999. Estimations
of the efficacy and reliability of paternity
assignments from DNA microsatellite
analysis of multiple-sire matings. Animal
Genetics 30: 355-361.
7. Lang, K.; Y. Yang; Y. Plante. 1996.
Fifteen polymorphic dinucleotide
microsatellites in llamas and alpacas. Animal
Genetics 27: 285-294.
8. Mommens, G.; A. Van Zeveren; L.
Peelman. 1998. Effectiveness of bovine
microsatellites in resolving paternity cases
in American bison, Bison bison L. Animal
Genetics 29: 12-18.
9. Morera, L.; D.F. De Andrés; M.
Barbancho; J.J. Garrido; C.J. Barba.
1999. Detección de variabilidad genética por
microsatélites en el Alano Español. Archivos
de Zootecnia 48: 63-70.
10. Pádár, Z.; B. Egyed; K. Kontadakis; L.
Zöldág; S. Fekete. 2001. Resolution of
parentage in dogs by examination of
microsatellites after death of putative sire:
case report. Acta Veterinaria Hungarica
49: 269-273.
11. Penedo, C.; R. Caetano; I. Cordova.
1998. Microsatellite markers for South
American camelids. Animal Genetics 29:
398-413.
12. Sam, C.; J. Schaaf; C. Lauk. 2001.
Improved breeding in camelids through
molecular techniques: Development of
STR multiplexes for identification and
parentage verification. En: Progress in
South American Camelids Research.
Proceedings of the 3rd European
Symposium and SUPREME European
Seminar. p 296-302. EAAP Publication
N° 105. Gerken M.; C. Reniere (eds).
Göttingen.
13. Sasse, J.; M. Mariasegaram; M.
Jahabar Ali; S. Pullenayegum; R.
Babu; J. Kinne; U. Wernery. 2000.
Development of a microsatellite
parentage and identity verification test
for dromedary racing camels. Abstracts
of the 27th Conference of the
International Society of Animal Genetics
(ISAG). Mineappolis, EE.UU.
14. Skidmore, J.; M. Billah; M. Binns; R.
Short; W. Allen. 1999. Hibridizing old
and new world camelids: Camelus
dromedaries x Lama guanicoe. Proc.
R. Soc. Lond. B 266: 649-656.
15. Vigilant, L.; M. Hofreiter; H. Siedel;
C. Boesch. 2001. Paternity and
relatedness in wild chimpanzee
communities. PNAS 98: 12890-12895.
____________________
(1) CONOPA
(2) E-mail: webmaster@conopa.org
(3) Department of Biodiversity and Ecological Processes, Cardiff University, Cardiff, U.K.
(4) Laboratorio de Microbiología y Parasitología Veterinaria, FMV-UNMSM
Email:rrosadioa@vetunmsm.edu.pe; rrosadio@terra.com.pe
|

